Biosimilaire ou générique
Attention : Biosimilaires ≠ génériques
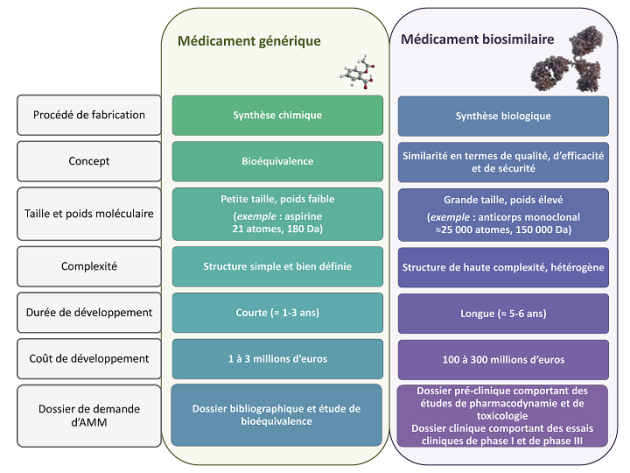
Les biosimilaires sont souvent assimilés, à tort, aux génériques. En effet des différences fondamentales existent.
"Les médicaments biosimilaires et les médicaments génériques ne sont pas comparables :
les matières premières utilisées, les procédés de production, les modes d'action, les procédures d'autorisation de mise sur le marché sont différents.
les réactions biologiques aboutissent à des produits qui doivent être étroitement contrôlés pour garantir une similarité entre le médicament biosimilaire et son biomédicament de référence."
Aussi, la durée et les coûts nécessaires pour développer un médicament biosimilaire sont bien plus importants que pour un médicament générique. En effet, les études requises pour l'obtention de l'autorisation des biosimilaires sont beaucoup plus poussées. Dans le cas des génériques, il est « seulement » nécessaire que le produit soit de qualité, et de démontrer qu'il y a une bioéquivalence avec le médicament princeps.
Remarque : Le cas particulier du tériparatide
Le 10 novembre 2020, un groupe générique a été créé pour le tériparatide, avec l'apparition de TERIPARATIDE BIOGARAN® comme générique de FORSTEO®, alors que le tériparatide appartient déjà à un groupe biologique similaire.
TERIPARATIDE BIOGARAN®est issu d'une synthèse chimique et une similarité avec le médicament de référence FORSTEO®, issu d'une technologie recombinante, a été démontrée.
TERIPARATIDE BIOGARAN® a donc reçu une AMM générique.